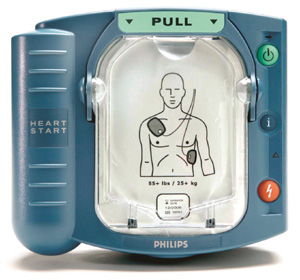
 필립스코리아가 지난 2002년부터 2013년까지 생산 판매한 저출력심장충격기에서 부품 불량에 따른 오작동 우려가 있어 보건당국이 안전 사용방법을 안내했다. 또한 보건당국은 국내에 수입된 3330개 제품에 대한 전수 점검에 나선다.
필립스코리아가 지난 2002년부터 2013년까지 생산 판매한 저출력심장충격기에서 부품 불량에 따른 오작동 우려가 있어 보건당국이 안전 사용방법을 안내했다. 또한 보건당국은 국내에 수입된 3330개 제품에 대한 전수 점검에 나선다.출산율 하락세 멈췄다…9년만에 깜짝 반등, 왜?
지난 9년간 내리막길을 걷던 합계출산율 추세가 반전될 조짐이다. 올해 3분기 합계출산율이 반등한 것으로 나타
 필립스코리아가 지난 2002년부터 2013년까지 생산 판매한 저출력심장충격기에서 부품 불량에 따른 오작동 우려가 있어 보건당국이 안전 사용방법을 안내했다. 또한 보건당국은 국내에 수입된 3330개 제품에 대한 전수 점검에 나선다.
필립스코리아가 지난 2002년부터 2013년까지 생산 판매한 저출력심장충격기에서 부품 불량에 따른 오작동 우려가 있어 보건당국이 안전 사용방법을 안내했다. 또한 보건당국은 국내에 수입된 3330개 제품에 대한 전수 점검에 나선다.#소아 알레르기 비염, 언제 왜 어떻게 일어나나? #글// 김지수 영동한의원 진료원장 코 알레르기는 소아 알레르기성 질환 중에서도 가장 귀찮은 병으로 꼽힌다. 일단 알레르기 비염에 걸리고나면 그 어린이는 정서적으로 산만�
#80세 이상 고령환자 인공관절 수술 가능하다. #글// 고용곤 연세사랑병원 병원장(정형외과 전문의) 한국은 이미 고령화 사회에 진입했다. 2050년에는 65세 이상 고령자가 전체 인구의 35% 이상 되는 ’초 고령사회’로 진입�
#언택트 시대에도 인간의 행태는 쉽게 바뀌지 않는다 #정신과 의사 기선완의 우리, 괜찮을까요? 글// 기선완 가톨릭관동대 국제성모병원 정신건강의학과 교수 코로나19 바이러스의 팬데믹 이후 비대면 언택트 시대가 오리라는
지난 9년간 내리막길을 걷던 합계출산율 추세가 반전될 조짐이다. 올해 3분기 합계출산율이 반등한 것으로 나타
유럽의회가 28일(현지시간) 러시아와 북한의 군사협력을 규탄하면서 한국의 우크라이나 지원을 촉구하는 내용의
정부의 상급종합병원 구조전환 시범사업이 속도를 내고 있는 가운데 지역 의과대학·병원 신설을 요구하는
걸그룹 뉴진스가 소속사 어도어와 전속 계약을 해지하겠다고 밝힌 가운데 ‘뉴진스’란 이름을 지키겠다
윤석열 대통령이 지난 27일 볼로디미르 젤렌스키 우크라이나 대통령의 특별사절단을 접견하고 북한군의 우크라
강원 춘천의 한 은행에서 전기 안전점검을 하던 공사 직원이 감전되는 사고가 발생했다. 28일 소방 당국에 따르
국회 본회의 상정을 앞뒀던 반도체특별법이 여야 간 이견으로 무산됐다. 국민의힘은 반도체 연구개발(R&D) 근
창원국가산업단지 미래경영자클럽은 28일 신화철강에서 올해 두번째로 1세대의 창업스토리와 노하우를 경청하는
한국항공전문학교 울진비행훈련원(이하 훈련원)이 국내LCC 항공사 에어서울과 조종자원 선발 및 양성을 위한 업
본격적으로 눈이 내리고 기온이 영하로 내려가며 식품업계는 연말 분위기를 풍성하게 해 줄 ‘겨울 에디션&rsq
최윤범 고려아연 회장이 울산 온산제련소를 찾아 임직원들을 격려하고, 김두겸 울산광역시장을 만나 감사 인사
코레일(한국철도공사)과 한국전력기술이 내부감사 혁신과 발전에 기여한 성과를 인정받아 ‘2024 한국감사인
4년 반 간의 공백기를 거쳐 팬들 곁으로 돌아오는 아이돌이 있다. 바로 넥슨 액션 역할수행게임(RPG) ‘엘소드&r
영플레이어상을 수상한 양민혁이 신인임에도 풀시즌을 치른 점에 대해 만족감을 드러냈다. 한국프로축구연맹






