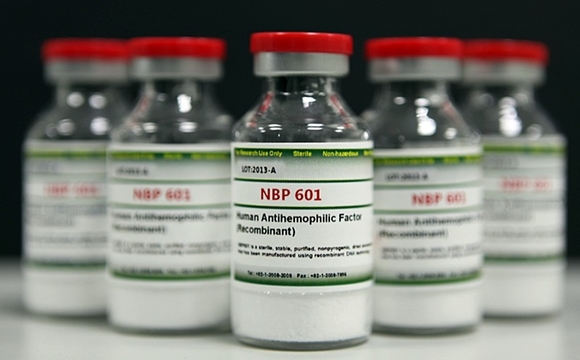
 [쿠키뉴스=조민규 기자] SK케미칼이 다국적 제약사 CSL사와 손잡고 만든 바이오 신약이 미국과 유럽에 이어 호주 시장까지 공략하며 글로벌 시장에서의 장악력을 넓혀가고 있다.
[쿠키뉴스=조민규 기자] SK케미칼이 다국적 제약사 CSL사와 손잡고 만든 바이오 신약이 미국과 유럽에 이어 호주 시장까지 공략하며 글로벌 시장에서의 장악력을 넓혀가고 있다.인천시 F1 유치 터무니없다…5억5000만원 ‘증발’ 위기
“타당성 조사를 하고 사업을 추진하겠다는 그 접근에서부터 ‘모터스포츠 모르는구나’ 하는 생각이
 [쿠키뉴스=조민규 기자] SK케미칼이 다국적 제약사 CSL사와 손잡고 만든 바이오 신약이 미국과 유럽에 이어 호주 시장까지 공략하며 글로벌 시장에서의 장악력을 넓혀가고 있다.
[쿠키뉴스=조민규 기자] SK케미칼이 다국적 제약사 CSL사와 손잡고 만든 바이오 신약이 미국과 유럽에 이어 호주 시장까지 공략하며 글로벌 시장에서의 장악력을 넓혀가고 있다.“타당성 조사를 하고 사업을 추진하겠다는 그 접근에서부터 ‘모터스포츠 모르는구나’ 하는 생각이
다음 달 16일 서울시교육감 보궐선거에 도전한 진보 계열 후보가 3명으로 압축됐다. 강신만 전 전교조 부위원장,
정부가 이달 초 발표한 연금개혁안이 시행되면 세대 경계 구간 연령은 최대 150만원의 보험료를 더 부담할 수 있
이재명 더불어민주당 대표는 국회에서 임현택 대한의사협회(의협) 회장과 만나 최근의 의정갈등 및 의료 차질과
‘영원한 재야’로 불리는 장기표 신문명정책연구원 원장이 22일 별세했다. 유족 등에 따르면 장 원장은
쿠키뉴스는 기성 언론의 책임과 사회 공헌을 실현하기 위해 대학언론인 활동을 후원하고 있습니다. 예비 언론인
북한은 1994년 김일성 사망 이후 고난의 행군 시기에 수많은 사람들이 굶어 죽는 처참한 상황에 처했다. 죽음의 공
전북특별자치도 주택가격이 전국 17개 광역지자체 중 최하위권의 낮은 가격으로 거래되는 것으로 조사됐다. 전북
토스증권이 개인투자자를 위한 리서치센터를 출범한다. 리포트 제공 대상을 개인투자자 중심으로 내세운 것이
국토교통부가 다음달 2일 ‘전세사기피해자 지원 및 주거안정에 관한 특별법’(전세사기특별법) 온라인 설
경북도는 소나무재선충병 피해 고사목 등의 정확한 분석과 신속한 대응을 위해 20개 시군을 대상으로 23일부터 내
배우 김고은과 노상현이 유쾌한 만남을 가졌다. 23일 서울 삼성동 메가박스 코엑스점에서 영화 ‘대도시의
세계유산의 향연 ‘2024 세계유산축전’이 23일부터 내달 6일까지 고령 지산동 고분군 일원에서 펼쳐진다. &
국내 유일의 지상무기 방위산업 전시회 ‘DX KOREA’가 올해 결국 둘로 나뉘어 열리게 됐다. 23일 방산업계에



