정부가 지난해 7월 발표한 ‘의료기기 규제혁신 및 산업육성방안(이하 의료기기 규제혁신방안)‘의 12개 세부과제 중 8개를 완료했으며, 나머지 과제도 올해 안으로 마무리 할 계획이라고 5일 밝혔다.
또 ‘의료기기 규제혁신방안’의 이행상황을 점검하고 현장에서 체감할 수 있는 방안을 추가로 발굴하기 위해 ‘의료기기 규제혁신 협의체’를 이달 중순부터 운영한다는 방침이다.
보건복지부와 질병관리본부, 식품의약품안전처에 따르면 남은 ‘의료기기 규제혁신방안’과제는 ▲규제과정의 그레이존 해소 ▲인허가 과정 실질적 원스톱 서비스 체계 구축 ▲혁신·첨단의료기술 조기 시장 진입 지원 ▲안전한 의료기기, 포괄적 네거티브 규제 등이다.
현행 의료기기 규제는 식약처 허가 → 요양급여·비급여 대상 확인 → 신의료기술평가 → 보험등재 심사 단계로 나눠져 있어 그간 의료기기 업체들은 규제단계별 정보를 종합적으로 이해하는데 어려움이 있었다.
이에 ‘의료기기 전 주기 통합상담 실시’와 ‘규제진행과정 내 신청인 참여강화 및 전문가 영입’ 및 ‘규제기준·결과 공개 강화 및 가이드북 개발’을 통해 규제과정의 그레이존을 해소한다는 방침이다.
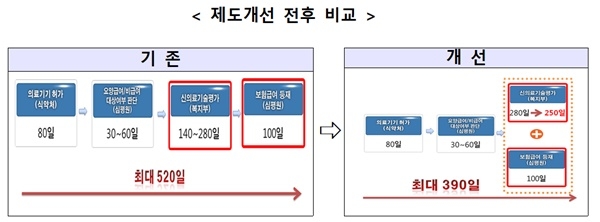
또 현행 의료기기 규제가 4단계로 진행됨에 따라, 신개발 의료기기의 시장진입기간(최대 520일)이 길고, 기관 간 중복 자료 요구가 발생했다. 이를 ‘신의료기술평가 대상심의 간소화 + 신의료기술평가-보험등재 동시 진행’과 ‘의료기기 허가-신의료기술평가 통합심사 전담팀 운영’을 통해 390일로 줄인다는 계획이다.
특히 인공지능(AI), 의료로봇, 3D 프린팅 등 첨단기술을 융합한 혁신의료기술은 새롭게 개발된 기술이므로 효과성에 대한 문헌적 근거가 부족하고, 시장 주기가 짧아 시장 진입이 지체될 경우 연구개발을 포기하는 경우가 있었다.
이를 ‘혁신의료기기 신속허가 가이드라인 개발’과 ‘예비코드 도입을 통한 조기시장 진입 절차 마련’ 및 ‘혁신의료기술 별도평가트랙 도입’, ‘혁신형 치료재료 가산수가체계 마련’을 통해 해소한다.
경미한 사항이 변경되는 체외진단기기에 대해서는 의료기기 업체가 자율적으로 변경하고, 안전성의 우려가 적은 체외진단검사에 대해서는 사후 신의료기술평가 방식을 단계적으로 적용할 예정이다.보건복지부 손호준 의료자원정책과장은 “지난해 발표했던 ‘의료기기 규제혁신방안’을 조속히 추진하는 동시에, 업체들이 참여하는 ‘의료기기 규제혁신 협의체’를 통해 현장에서의 애로 사항을 점검할 계획이다”라고 밝혔다.
유수인 기자 suin92710@kukinews.com