현재까지 미국을 비롯해 전 세계에서 에볼라 치료제와 백신은 없다. 하지만 인간의 생명을 위협하는 절체절명의 위기 속에서 실험 약물을 사용할 수 있다면 어떻게 해야 할까. 미국은 이러한 상황에서 과감하게 사람에게 임상이 시행되지 않은 치료제를 직접 투약하는 처방을 내렸다.
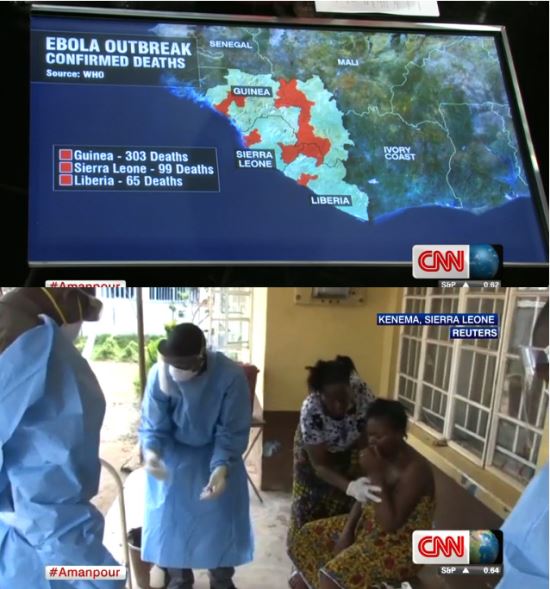
서아프리카 등을 중심으로 치사율이 최대 90%로 ‘죽음의 바이러스’로 알려진 에볼라 바이러스가 급속하게 퍼지고 있음에 따라 미국 식품의약품(FDA)이 승인받지 않은 치료제라 하더라도 긴급하게 사용을 허락하는 방안을 검토하고 있는 것으로 알려져 전 세계적인 관심이 모아지고 있다.
5일 CNN 등 주요 외신에 따르면 미국 스테파티 야오 FDA 대변인은 “FDA가 승인받지 않은 치료제라 하더라도 긴급한 사용을 허락하는 방안을 검토하고 있다”고 밝혔다.
◇에볼라 치료 약물 ‘FDA 승인 전 사용’, 치료 효과 보여
에볼라 바이러스의 치사율은 무려 90%다. 올해 3월부터 에볼라 바이러스로 인한 사망자가 700명을 넘어섰다. 이러한 사태의 심각성을 고려한 미국은 사람에게 임상이 시행되지 않은 치료제를 직접 투약하는 긴급 처방을 내렸다. 미국 국립보건원(NIH)과 질병통제예방센터(CDC)는 라이베리아에서 구호활동 중인 에볼라 바이러스에 감염된 켄트 브랜틀리와 낸시 라이트볼 등 미국인 치료제를 투약했다.
에볼라 바이러스의 치료제를 개발한 것은 직원이 9명에 불과한 제약회사라고 CNN 방송 등이 보도했다. 미국 샌디에이고에 있는 ‘맵 바이오제약(Mapp Biopharmaceutical)’은 지난 2003년 전염병 치료제와 백신 개발을 목표로 설립된 회사다.
맴 바이오제약이 개발한 ‘지맵(ZMapp)’은 에볼라 바이러스에 대항하는 면역 시스템을 형성하도록 도와주는 단일클론항체들을 혼합해 만든 일종의 칵테일 치료제다. 이 치료제는 원숭이를 대상으로 한 동물실험에서 효능을 보였지만 아직까지 인간을 대상으로 한 임상시험은 시행된 적이 없다.
하지만 인간에게 임상 시험을 하지 않은 지맵은 효과를 발휘했다. 치료제 처방 후 상태가 호전된 브랜틀리는 지난 2일 미국으로 돌아와서 조지아주 애틀랜타의 에모리대학 병원에서 격리치료를 받고 있으며, 라이트볼은 5일 미국에 도착해 같은 병원에서 치료받을 예정이다.
◇미국 ‘시도할 수 있는 권리 인정’, FDA 승인 전 약물 사용 허용
미국에서는 말기암 환자 등을 위해 일부 주에서 FDA 승인이 없더라도 임상시험 중인 신약을 사용할 수 있도록 하는 ‘시도할 수 있는 권리(Right to Try) 법안’이 마련돼 있다.
콜로라도 주지사는 지난 5월 미국에서 FDA 승인이 없더라도 임상시험 중인 신약을 사용할 수 있도록 하는 법안에 서명했다고 AP통신 등이 전했다. 새 법은 FDA의 복잡하고 까다로운 승인 절차를 생략하고 임상시험을 하고 있는 약을 치료에 사용할 수 있도록 하는 내용을 담고 있다.
말기암, 치료제가 없는 질병 등에 대해 마지막 희망이라도 잡고 싶은 환자 등에게 의사의 처방만으로 제약사에 신약 사용을 요구할 수 있다.
당시 법안을 주도했던 조앤 지널 콜로라도주 하원의원은 워싱턴포스트(WP)를 통해 “죽음에 직면한 모든 사람들에게 가능한 모든 약물을 써볼 수 있는 기회를 줘야 한다”고 주장했다.
우리나라에서도 이러한 신약이 개발될 경우에 대비해, 시판 전 약물 승인 등에 대해 심도 있는 고민을 해봐야 한다는 주장도 있다. 한 제약업계 관계자는 “대 테러전, 각종 감염병 등 국가 긴급 사태에 대비해 승인 전 약물이라도 긴급 상황에서는 처방할 수 있는 법 조항이 마련될 수 있어야 한다”고 언급했다.
하지만 여전히 안전성이 입증되지 않은 약물에 대해 부작용을 우려하는 목소리도 높다. 인간에게 임상을 해보지 않거나, 안전성이 검증되지 않은 약물을 사전에 허가할 경우 국가 기관의 신뢰가 무너질 수 있기 때문이다. 실제 당시 이러한 법안 논의 과정에서 미국 FDA는 “안전성과 효능이 입증되지 않은 치료제를 허할 경우에 대중을 보호하는 기관의 임무가 약화될 우려가 있다”는 성명을 발표한 바 있다.
장윤형 기자 vitamin@kukimedia.co.kr