알츠하이머병은 뇌 신경세포가 점차 손상되면서 기억력, 사고력 등 인지 기능이 서서히 저하되는 대표적 퇴행성 뇌질환이지만, 아직 근본적 치료제가 없는 상황이다.
현재 알츠하이머병은 주로 PET·MRI를 활용한 영상장비로 진단한다.
이는 회당 높은 검진비용이 소요되고, 질환이 일정수준 이상 진행한 후에야 영상관측이 가능해 발병 초기 감지하기 어려운 것도 단점으로 꼽힌다.
간단 체외진단으로 알츠하이머 판독
한국표준과학연구원(KRISS)이 분자가 가진 고유 광학신호를 수억 배 증폭해 체액에 있는 극미량의 알츠하이머병 생체지표를 정확히 검출하고 정량화하는 진단플랫폼을 개발했다.
이 기술은 간단한 체액검사만으로 생체지표들을 초고감도·고신뢰도로 정량 검출할 수 있어 기존 영상진단법의 한계를 보완하고, 질병의 조기 진단과 치료 모니터링에 활용할 수 있을 전망이다.
‘아밀로이드베타(Aβ)’는 알츠하이머병의 주요 병리적 특징인 단백질 조각(펩타이드)으로, 뇌 속에 비정상적으로 축적돼 신경세포 손상과 인지기능 저하를 유발하는 것으로 알려져 있다. 특히 펩타이드 Aβ42와 Aβ40은 알츠하이머병과 밀접한 연관이 있는 생체지표다.
이 두 펩타이드를 검출해 비율을 산출하면 알츠하이머병의 진행도를 조기 진단할 수 있다.
그러나 기존 분석 방식인 효소면역측정법(ELISA)은 혈액이나 뇌척수액 등 체액에 들어있는 극저농도의 두 펩타이드를 동시에 정확히 검출하기 어려웠다.
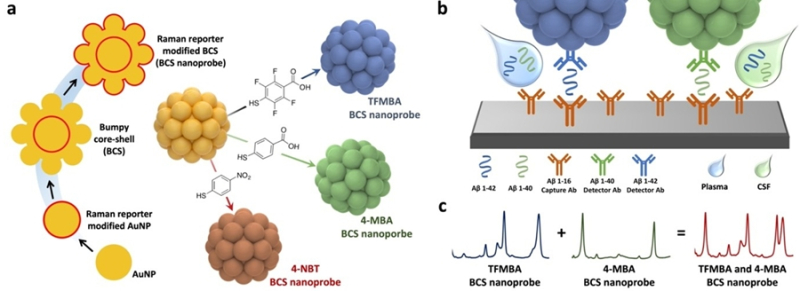
KRISS 의료융합측정그룹은 기존 체액 검사 방식보다 약 10만 배 이상 민감하면서 여러 생체지표를 정확히 구별해 정량 측정할 수 있는 ‘표면증강 라만분광법(SERS) 기반 초고감도 다중 정량 검출 플랫폼’을 개발했다.
SERS는 빛이 분자와 만나 생기는 고유한 신호를 금속 나노구조로 증폭, 극히 적은 양의 분자까지도 정확히 검출할 수 있다.
연구진은 단일 입자에서 강하고 균일한 SERS 신호를 개별 감지할 수 있는 해바라기 모양 단면의 식별 가능한 다종 금 나노입자를 개발했다. 이는 기존 구형 금 나노입자의 입자 간 거리에 따른 불균일한 신호 문제를 극복하고, 입자 내부와 표면 전체에 고밀도로 균일한 신호 증폭 지점을 형성해 단일 입자에서도 강하고 재현성 높은 신호를 구현할 수 있다.
이를 통해 표적물질 농도에 비례하는 우수한 정량성을 확보하고, 서로 다른 표적물질을 동시 검출할 수도 있다.
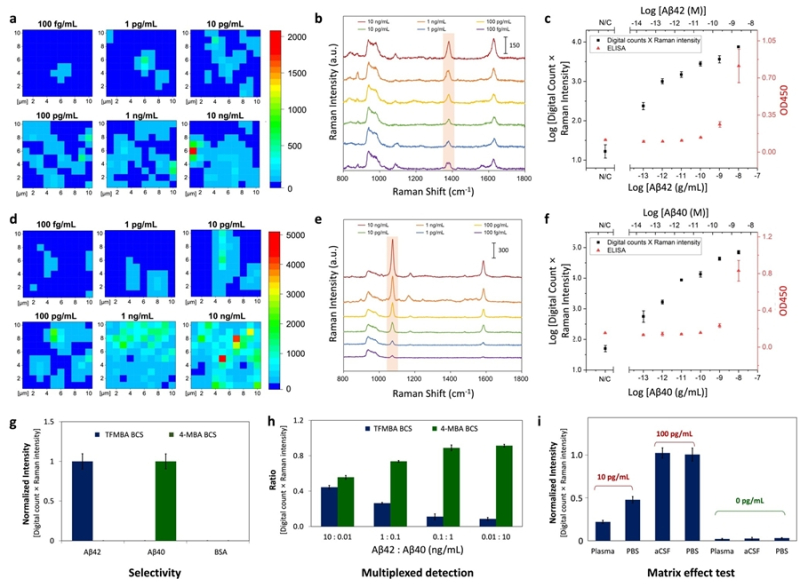
연구진은 고유 ID를 부여한 다중검출용 SERS 나노입자를 적용해 Aβ42와 Aβ40을 검출한 결과 천조 분의 1그램 이하 수준인 8.7×10-17g/mL, 1.0×10-15g/mL을 정량 검출하는 데 성공했다.
KRISS 의료융합측정그룹 유은아 책임연구원은 “이번에 개발한 검출 플랫폼은 저비용으로 대량생산이 가능하고, 다양한 생체지표에 유연하게 적용할 수 있다”며 “알츠하이머병뿐만 아니라 암, 뇌 질환, 감염병 등 다양한 질환의 조기·신속 체외 진단 및 모니터링에 활용할 수 있어 범용성이 높고 상용화에 유리한 기술”이라고 말했다.
한편, 이번 연구성과 국제학술지 지난 4월 ‘Biosensors & Bioelectronics(IF: 10.5)’에 게재됐다.































